الملخص
*-إزالة المنجنيز من المياه الجوفية عن طريق الأكسدة مع (KMNO4) يكلف الكثير من المال.
*-تكاليف عالية تجعل الشركات تعانى من خسائر مالية فى عملية معالجة المياه .
* ونحن سوف تظهر كيفية القيام بهذا العمل مع خفض التكاليف.
* سوف يتم ذلك بطريقة تقلل من التكلفة المالية.
مقدمة
الحديد، والمنغنيز إلى ، هي بعض من العناصر الأكثر وفرة في القشرة الأرضية. وهي توجد في المياه المنبثقة من الرشح التربة والتلوث الصناعي. هذه العناصر لا تشكل أي خطر على صحة الإنسان أو على البيئة. لكنها تسبب الازعاج .
الحديد والمنجنيز يعطي لون المياه التي يمكن وصمة على الكتان والأدوات الصحية. ، وعندما لايتم القضاء عليها، يمكن أن تتأكسد تدريجيا في شبكة التوزيع إعطاء لون الماء، الطعم، والرائحة، والتعكر لصالح التنمية من الكائنات الحية الدقيقة مع عواقب وخيمة بالنسبة للمستخدمين. في المياه السطحية أو الأرض، يجد المرء الحديد والمنجنيز في أشكال كيميائية مختلفة (المنحلة، أو المعقد) في تركيزات متغير (مينت وباري، 1999؛ أوموريجي وآخرون، 2002؛. موانجا وBarifaidjo، 2006). ويمكن أن تكون موجودة في تركيزات من أجل من 2-5 ملجم / لتر من الحديد و0،5-2 ملغ / لتر من المنغنيز (إليس وآخرون، 2000؛. Roccaro وآخرون، 2007) أو التي هي أعلى بشكل ملحوظ وقادرة على تحقيق 20ملغم / لتر الحديد و 5 ملغم / لتر المنجنيز (Berbenni وآخرون، 2000). طرق إزالة الحديد والمنجنيز من المياه الإزالة عبارة عن تحويل الأشكال الذائبة من الحديد الثنائى والمنجنيز الثنائى عن طريق الأكسدة، إلى رواسب هيدروكسيد الحديد وثانى أكسيد المنجنيز ، يليه عن طريق الترشيح.
يمكن أن يتم أكسدة خارجية باستخدام عوامل تأكسد كيميائية قوية مثل الأكسجين والكلور وثاني أكسيد الكلور، والأوزون أو برمنجنات البوتاسيوم (العربى وآخرون، 2009؛. Katsoyiannisa وآخرون، 2008) أو بيولوجيا (Katsoyiannisa وآخرون، 2008؛. تشين وآخرون .، 2009؛ Tekerlekopoulou وآخرون، 2008؛. Tekerlekopoulou وVayenas، 2007؛ Burgera وآخرون، 2008). .
وكان الهدف من هذا العمل إلى دراسة عملية لوجدت طريقة للحد من تكاليف إزالة الحديد والمنجنيز .أكسدة المنغنيز والحديد الاستخدام الرئيسي للبرمنجنات هو إزالة الحديد والمنجنيز. سوف تقوم برمنجنات البوتاسيم بأكسدة الحديد والمنجنيز لتحويل الحديد (2 +) إلى الحديديك (3 +) والمنغنيز الثنائى إلى المنجنيز الرباعى. فإن الأشكال تتأكسد و تترسب كما فى هيدروكسيد الحديديك وهيدروكسيد المنغنيز (عوا، 1991).
فإن التركيب الكيميائي الدقيق للراسب تعتمد على طبيعة الماء، ودرجة الحرارة، ودرجة الحموضة.
المعادلة الكيميائية الكلاسكية لعملية الأكسدة للحديد والمنجنيز هى

ويستهلك ذلك من خلال إنتاج حامض يتفاعل مع القلوية بمعدل 1.49 ملغم / لتر كما كربونات الكالسيوم CaCO3 لكل ملغم / لتر من الحديد +2 و1.21 ملغم / لتر كما كربونات الكالسيوم CaCO3 لكل ملغم / لتر من المنجنيز +2 أكسدة. وينبغي النظر في هذا الاستهلاك من القلوية عندما يتم استخدام العلاج ببرمنغنات جنبا إلى جنب مع الشبة ، الأمر الذي يتطلب أيضا القلوية لتشكيل رواسب.
الجرعة من برمنجنات البوتاسيوم اللازمة للأكسدة هو 0.94 ملغ / ملغ حديد و 1.92 ملغ / ملغ المنغنيز (كولب / Wesner / كولب، 1986). في الممارسة العملية، تم العثور على القيمة الفعلية من برمنجنات البوتاسيوم التى تستخدم ليكون أقل من ذلك .
ويعتقد أن هذا هو بسبب تأثير حفاز من MnO2 على ردود الفعل (أوكونيل، 1978). الوقت اللزم للأكسدة تتراوح من 5 إلى 10 دقائق، شريطة أن يكون الرقم الهيدروجيني هو أكثر من 7.0 (كاوامورا، 1991).
مساهماتي هو لتقليل كمية من برمنجنات البوتاسيوم عن طريق تعديل PH بواسطة هيدروكسيد الصوديوم.
المشكلة محل البحث
فى المعادلة الكلاسيكية للتخلص من المنجنيز نلاحظ ما يلى
![]()
هذا يعنى أنة عندما يكون تركيز المنجنيز فى الماء( 1.2 جزء لكل مليون جزء) هذا يعنى أننا نحتاج( 0.0023 جم) للتر وهذا يترتب علية اننا نجتاج (2.3 كجم ) للمتر المكعب
ثمن كيلو البرمنجنات فى مصر حوالى 140 جنية مصرى مما يدل على مدى التكلفة المادية.
فكرتى فى هذا البحث
برمنجنات البوتاسيم لها أثران
- أثر تعقيمى تزداد قيمتة فى الأوساط الحامضية.
- أثر تأكسدى تزداد قيمتة فى الأوساط القاعدية.
(Cleasby et al., 1964 and Wagner, 1951).
التفاصيل
يتم رفع الأس الهيدروجينى لتقليل كمية البرمنجنات المستخدمة فى الأكسدة
يتم إضافة برمنجنات البوتاسيم تركيز (1 مولارى) إلى مياة جوفية تركيز المنجنيز بها (1.2 جزة لكل مليون جزء) ويتم قياس تركيز المنجنيز بعد رفع قيمة الاس الهيدروجينى عن طريق هيروكسيد صديوم (1 عيارى) .

لاحظ
تفاعل البرمنجنات مع المنجنيز والحديد يستهلك قلوية المياة بمعدل (1.49 جزء للمليون )فى حالة الحديد و 1.21( جزء للمليون) فى حالة المنجنيز هذا يعنى أنة لا توجد خطورة من عملية رفع الأس الهيدروجينى لأنة سوف ينخفض القليل من تلقاء نفسة
العملى بالرسم.
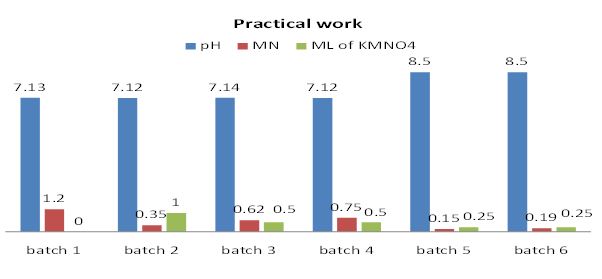
ولتقليل الإستهلاك أكثر تم عمل هذة التجربة بتركيزات أخرى قللت الأستهلاك سوف يتم عرضها لاحقا
. الاستنتاجات
. يمكن أن تقلل من كمية KMNO4 المستخدمة لإزالة الحديد +2 والمنجنيز +2 في المياه الجوفية عن طريق إضافة هيدروكسيد الصوديوم إلى زيادة الأس الهيدروجينى والذى يؤدى الى زيادة قدرة KMNO4 على الأكسدة.
References
*-Myint and Barry, 1999; Omoregie et al., 2002; Muwanga and Barifaidjo, 2006).
*-Ellis et al., 2000; Roccaro et al., 2007
*-Berbenni et al., 2000
*-El Araby et al., 2009; Katsoyiannisa et al., 2008
*-Katsoyiannisa et al., 2008; Qin et al., 2009; Tekerlekopoulou et al., 2008; Tekerlekopoulou and Vayenas, 2007; Burgera et al., 2008.
*-AWWA, 1991
*-Culp/Wesner/Culp, 1986
*-O’Connell, 1978
*-Kawamura, 1991
*-Cleasby et al., 1964 and Wagner, 1951).
*- potassium permanganate chapter 5.
إعداد كيميائى / علاء احمد محمد سيد
كيميائى بشركة مياة الشرب والصرف الصحى بسوهاج.




